Escuchar esta nota
Detenido
La cifra impresiona: cerca de 12 000 pacientes han sido diagnosticado con una condición llamada “hongo negro” en India, la mayoría de ellos enfermos que se están recuperando de covid-19. Esta rara infección puede llegar a ser letal, con una tasa de mortalidad cercana al 50%. Una cifra que preocupa no sólo al mundo científico, sino a todas las comunidades donde se han presentado casos (uno, por ejemplo, se registró la semana anterior en Uruguay). En México, Gregorio Avendaño Jiménez, primer paciente sospecho de hongo negro, murió el pasado lunes debido a las complicaciones de la enfermedad. ¿Qué es y cuál es el hábitat perfecto para que este hongo desarrolle una enfermedad grave e, incluso, mortal? Raúl Rivas González y María Francisca Colom Valiente nos hablan de él…
¿Qué es la mucormicosis, la infección que está causando estragos en la India?
Raúl Rivas González
En medio de la pandemia, la India ha informado que sufre de un número inusualmente alto de casos de mucormicosis, y que más del 80% de los pacientes necesitan cirugía de inmediato porque la tasa de mortalidad puede alcanzar el 94%.
¿Pero qué tiene que ver esta enfermedad con la covid-19? Se trata de una infección micótica oportunista causada por diversas especies de hongos pertenecientes al orden Mucorales y que, en el caso de la India, puede estar asociada a los altos índices de infección por covid-19 que sufre el país. ¿Por qué? Porque los mucorales se consideran patógenos oportunistas, lo que significa que requieren de un sistema inmunológico suprimido u otra afección subyacente. Tan frecuentes son que podríamos estar hablando de la tercera causa más común de infección fúngica invasiva en pacientes inmunodeprimidos.
Hasta la fecha, las mucormicosis han sido asociadas a una alta morbilidad y mortalidad. De hecho, los mucorales puede causar infecciones letales en una población más amplia y heterogénea que otros hongos oportunistas.
Actualmente se conocen 27 especies diferentes de mucorales, distribuidas en 11 géneros que han sido identificadas como agentes causales de la mucormicosis. La más frecuente es la especie Rhizopus arrhizus, que aparece en el 70% de todos los casos.
La mucormicosis no se transmite de persona a persona, y puede ser adquirida por diferentes vías.
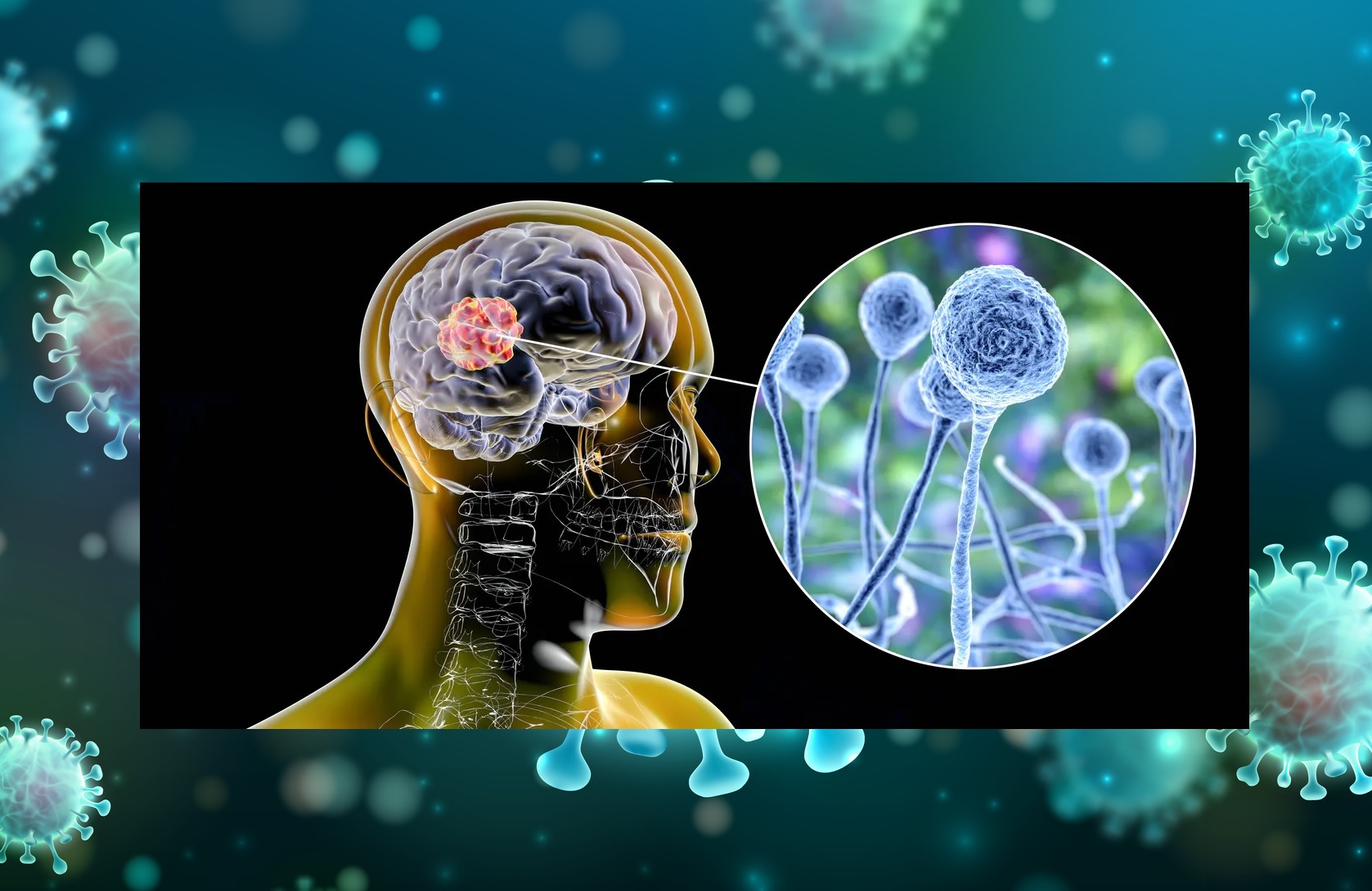
• La nariz, los senos nasales, los ojos y el cerebro se infectan con mayor frecuencia causando una infección grave denominada mucormicosis rinocerebral, que suele ser mortal.
• Cuando se inhalan las esporas pueden invadir los pulmones y causar mucormicosis pulmonar.
• El tracto digestivo se infecta al ingerir las esporas, lo que ocasiona la mucormicosis gástrica.
• Una cuarta forma de la infección ocurre al entrar las esporas a través de una ruptura en la piel, lo que da lugar a la llamada mucormicosis cutánea.
• La quinta forma de la enfermedad recibe el nombre de mucormicosis diseminada, y la sexta variante es una miscelánea de otros tipos que puede causar endocarditis (inflamación del revestimiento interno de las cámaras y válvulas cardíacas) u osteomielitis (infección ósea), entre otras complicaciones.

Una vieja conocida
La enfermedad fue descrita por primera vez en 1876 en Alemania por Paul Fürbringer tras examinar a una paciente que murió de cáncer. En su pulmón derecho mostraba gran cantidad de hifas de hongos y algunos esporangios.
Poco después, en 1885, Arnold Paltauf publicó el primer caso de mucormicosis diseminada, al que denominó “micosis mucorina”. Con el tiempo, se diagnosticaron más casos, y la incidencia de la enfermedad no ha dejado de crecer desde entonces.
(Por ejemplo: en España, en el año 2005 se contabilizaron 0,43 casos por millón de habitantes y 0,62 casos por cada 100 000 admisiones hospitalarias. En la vecina Francia, la incidencia se duplicó del año 1997 al 2006 y en Bélgica la incidencia se multiplicó por 10 en tan sólo una década.)
Actualmente se estima que la incidencia de este tipo de infecciones en países con registros validados es de aproximadamente 1 a 1,5 casos por millón de habitantes/año.
En general, la infección causa dolor, fiebre, a veces tos y genera daños tisulares graves con rápida destrucción de los tejidos hasta llegar a originar necrosis severa.
La probabilidad de sufrir mucormicosis aumenta en pacientes diabéticos e inmunocomprometidos. Los hongos mucorales infectan a individuos inmunodeprimidos con factores de riesgo predisponentes, incluidos diabetes no controlada, quimioterapia, enfermedades hematológicas, trasplante de órganos, niveles elevados de hierro en sangre o terapia con corticosteroides, entre otros.
La prevalencia es 70 veces mayor en la India
Según algunos análisis, la India es el país más afectado por la mucormicosis y contribuye con más del 40% de todos los casos notificados en el mundo. La prevalencia estimada de la mucormicosis es alrededor de 70 veces mayor en la India que en los datos globales. Los factores de riesgo que la predisponen en la India pueden incluir condiciones socioeconómicas, malas condiciones higiénicas y la alta prevalencia de diabetes mellitus en la población.
De acuerdo a los datos disponibles, en la India los pacientes con tuberculosis pospulmonar y enfermedad renal crónica tienen un riesgo adicional de desarrollar mucormicosis. La mayoría de las personas con ésta, o sospecha, son tratadas con dosis altas de anfotericina B que es administrada por vía intravenosa. El isavuconazol, por vía oral o por vía intravenosa, es una alternativa y el posaconazol también puede ser efectivo, especialmente como terapia de consolidación.
Aunque Rhizopus arrhizus es el agente etiológico más común de la mucormicosis en la India, están aumentando las infecciones por otros hongos. El amplio espectro de agentes implicados en la mucormicosis enfatiza la necesidad de mejorar las rutinas clínicas y determinar la prevalencia exacta de la enfermedad en diversas poblaciones en riesgo.
No hay que olvidar que el diagnóstico y el tratamiento tempranos de la mucormicosis son esenciales para prevenir la muerte o para evitar una cirugía extensa, que a menudo causa desfiguración facial.
◾◾◾
Mucormicosis: ¿por qué afecta a los pacientes de coronavirus?
María Francisca Colom Valiente
Después de más de un año de pandemia, las noticias sobre el coronavirus y sus consecuencias nos resultan tan cotidianas que no esperábamos más sorpresas. Ahora sólo observamos un lento transcurrir hacía la anhelada y liberadora inmunidad de rebaño cubierta por las vacunas.
Sin embargo, la pesadilla nos ha sorprendido (otra vez) con un mal sueño: los hongos que invaden a las más desafortunadas víctimas de este descalabro, la mucormicosis. Se trata de una enfermedad muy rara en todo el mundo y algo menos extraña en la India. En este país, su incidencia ha aumentado mucho entre pacientes que sufren covid-19.

¿De dónde salen estos hongos?
La mucormicosis es una enfermedad producida por hongos microscópicos (mohos) del orden de los Mucorales. Tienen pigmentos oscuros y viven en los suelos ricos en vegetación, en materia orgánica y en sustratos como el abono o compost.
Aunque podemos considerarlos cosmopolitas, son más frecuentes en zonas cálidas y húmedas. La India es el país que siempre ha tenido la incidencia más alta de esta enfermedad.
Son hongos “oportunistas”, dado que sólo provocan enfermedad en personas con déficit de defensas, como los diabéticos descompensados, los que padecen leucemia o han recibido un trasplante.
Es decir, para que estos hongos produzcan una enfermedad, necesitan que nuestras defensas estén lesionadas o tengan un problema de funcionamiento, ya sea permanente o transitorio.
¿Qué necesitan estos hongos para desarrollar una enfermedad?
Cuando estos hongos contactan con los epitelios (la piel o las mucosas) intactos, no son capaces de penetrar ni de colonizarlos. En estos casos, se eliminan por arrastre con la descamación y las secreciones.
Si llegan a través de una herida en la piel, por aspiración hacia la nariz o más profundamente en el pulmón, intentan adaptarse al entorno y sobrevivir. Pero ahí las defensas celulares (los leucocitos y macrófagos) los destruyen en cuanto los reconocen como agentes extraños.
De modo que, para conseguir una invasión efectiva y desarrollar una enfermedad grave, se tienen que dar una serie de circunstancias excepcionales y facilitadoras.
Veamos qué es lo que está sucediendo a los pacientes de coronavirus en la India.
La India es un país cálido y húmedo que favorece a estos hongos. Además, tiene uno de los mayores índices de malnutrición del mundo. Esto significa que buena parte de la población tiene una salud precaria y defensas debilitadas.
Sobre esta base se suman otros problemas frecuentes como la diabetes descompensada. Los pacientes diabéticos mal controlados tienen un elevado riesgo de desarrollar infecciones. De hecho, el perfil de muchos pacientes con mucormicosis en la India corresponde a una persona malnutrida, con diabetes mal controlada y que ha adquirido covid-19.
El tratamiento contra el coronavirus favorece las afecciones de mucormicosis
Entonces nos preguntamos, ¿por qué golpea a los pacientes de coronavirus? Sabemos que en los casos de covid-19 con evolución severa o grave, se produce una reacción inflamatoria muy agresiva, la tormenta de citoquinas, en la que estas moléculas defensivas atacan los propios tejidos.
La única medicación disponible para controlar este fenómeno es el uso de los glucocorticoides o corticoesteroides. Estos fármacos bloquean la respuesta defensiva celular (leucocitos y macrófagos) y molecular (citoquinas).
Con ellos evitamos el autoataque que induce el coronavirus en nuestros tejidos. Sin embargo, al mismo tiempo paralizamos las células y moléculas que impiden que los hongos infecten.
En resumen, tenemos la siguiente situación: un individuo con epitelios frágiles o heridos (causa de la malnutrición), que además tiene una inmunidad poco eficiente por diabetes u otra patología, al que se le bloquea la respuesta de citoquinas y macrófagos mediante corticoides. En esta circunstancia, los hongos mucorales abundantes en el ambiente pueden invadir sus tejidos y provocar la enfermedad.
Un hábitat ideal para el hongo negro
Cuando todas las situaciones se dan de forma simultánea, se crea un hábitat en el que no hay impedimentos para que estos hongos se desarrollen. Así, invaden los tejidos con una progresión imparable.
Habitualmente empiezan en la nariz, invaden la órbita ocular y penetran hasta cerebro. Además, estos hongos son angioinvasores, buscan los vasos sanguíneos y se desarrollan y diseminan por ellos, taponándolos en su crecimiento.
Esto hace de la mucormicosis una enfermedad muy agresiva y compleja de tratar con éxito. Los taponamientos dejan sin riego sanguíneo el tejido y no permiten una adecuada difusión de fármacos a los mismos.
La mortalidad de estos procesos es obviamente elevada y más si los recursos sanitarios son escasos. En definitiva, esta es otra de las situaciones que nos llevan a entender la importancia de tener servicios de salud robustos, eficientes y universales, que contemplen a todos los individuos y al entorno.
Raúl Rivas González. Catedrático de Microbiología en la Universidad de Salamanca. Licenciado en Biología (1999) y doctor en Microbiología (2003).
María Francisca Colom Valiente. Profesora Titular de Microbiología en la Universidad Miguel Hernández. Gran parte de su trayectoria investigadora está dedicada al estudio de hongos patógenos humanos y animales.
Fuente: The Conversation.




